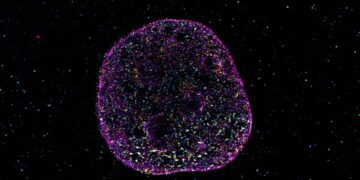
اخیرا محققان سلولهایی را که قادر به تشکیل سلولهای پشتیبان تخصصی مغز هستند، به مغز موش پیوند زدند.
به گزارش تکناک، محققان متوجه شدند که آنها نه تنها با سلولهای ناسالم، بلکه با سلولهای مسن نیز رقابت میکنند و جایگزین آنها میشوند. این یافته ها راه را برای توسعه درمان موثر برای طیف وسیعی از بیماری ها مانند مولتیپل اسکلروزیس، ALS، بیماری آلزایمر، اوتیسم و اسکیزوفرنی باز می کند.
سلول های گلیال یک اصطلاح برای سلول هایی است که به عنوان یک سیستم پشتیبانی برای سلول های عصبی یا همان نورون ها عمل می کنند. سلول های پیش ساز از نسل سلول های بنیادی هستند که می توانند به انواع سلول های خاص تمایز یابند. در مورد سلول های گلیال، سلول های پیش ساز گلیال انسانی (hGPCs) به زیرگروه هایی از جمله آستروسیت ها و الیگودندروسیت ها که برای عملکردهای خاص تخصص دارند، تمایز می یابند.
آستروسیت ها اکثر سلول های سیستم عصبی مرکزی ما را تشکیل می دهند و از نورون ها پشتیبانی و محافظت می کنند، مواد مغذی را حمل می کنند و مواد زائد را از بین می برند. الیگودندروسیت ها پوشش عایق و غنی از چربی به نام میلین را در اطراف برخی آکسون ها قرار می دهند و آن را حفظ می کنند. آکسون بخشی از نورون است که به نورون دیگری متصل می شود و امکان انتقال تکانه های عصبی را فراهم می کند.
آستروسیت ها و الیگودندروسیت های ناکارآمد، با چندین بیماری عصبی و عصبی-روانی مرتبط هستند. با توجه به توانایی hGPC ها برای ایجاد آستروسیت ها و الیگودندروسیت های جدید، محققان دانشگاه کپنهاگ، نحوه پیوند hGPC های سالم را بررسی کرده اند تا متوجه شوند چگونه می تواند به بازیابی عملکرد مغز کمک کند.
محققان قبلاً نشان داده بودند که سلولهای گلیال انسان سالم با پیوند سلولهای گلیال ناسالم موش به موش های مبتلا به بیماری هانتینگتون که یک بیماری ارثی نادر و کشنده است که باعث تخریب پیشرونده نورون میشود، جایگزین میشوند.
در مطالعه حاضر، آنها می خواستند ببینند که آیا سلول های انسان سالم می توانند جایگزین سلول های انسان بیمار شوند یا خیر. بنابراین آنها hGPC های سالم را به موش های «کایمریک» معرفی کردند که سلول های بنیادی مشتق شده از انسان های مبتلا به بیماری هانتینگتون به آنها تزریق شده بود. محققان متوجه شدند که سلول های سالم به طور کامل جایگزین سلول های بیمار شده اند.
استیون گلدمن، نویسنده مسئول این مطالعه گفت: ما سلولهای سالم انسانی را به موشهایی پیوند زدیم که با گلیال جهشیافته هانتینگتون «انسانسازی» شده بودند و خوشبختانه سلولهای گلیال سالم پیشی گرفتند و جایگزین گلیال بیمار شدند و در واقع جمعیت گلیال بیمار را ریشه کن کردند.
جالب اینجاست که محققان متوجه شدند زمانی که hGPCهای اهداکننده جوانتر به مغز موشهای انسانسازی شده وارد شدند، با سلولهای سالم و غیر بیمار، اما مسن رقابت کردند و جایگزین آنها شدند. محققان می گویند که یافته های آنها مبنی بر اینکه hGPC های سالم جایگزین سلول های بیمار و پیر شده اندف بسیار قابل توجه است و پتانسیل ایجاد درمان هایی را نشان می دهد که می توانند در طیف وسیعی از بیماری ها مورد استفاده قرار گیرند.
گلدمن میگوید: یافته های این مطالعه به ما نشان داد که فقط بحث سلولهای سالم رقیب سلولهای بیمار بیماری هانتینگتون نیست، بلکه از نظر استفاده، کاربرد آن بسیار گستردهتر است، زیرا ما میتوانیم به انواع اهداف بیماری که در آنها جمعیت گلیال مسنتر یا بیمار را داریم، وارد شویم.
سلول های گلیال برای ایجاد برخی از آسیب شناسی های عصبی حیاتی هستند. بیماری های نورودژنراتیو اسکلروز جانبی آمیوتروفیک (ALS) که به عنوان بیماری های لو گریگ، صرع، مولتیپل اسکلروزیس (MS)، بیماری پارکینسون و بیماری آلزایمر نیز شناخته می شود، با سلول های گلیال ناکارآمد مرتبط است. اختلالات عصبی روانی، اختلال طیف اوتیسم (ASD)، اختلال دوقطبی و اسکیزوفرنی از دیگر بیماری های این دسته می باشند.
گلدمن گفت: اگر بتوانیم سلولهای بیمار و پیر را جایگزین کنیم، باید بتوانیم جنبههایی از عملکرد طبیعی را در این بیماریهای مغزی بازیابی کنیم.
محققان می خواهند آزمایش های بیشتری را برای بررسی اثربخشی پیوند hGPC در بیماری هانتینگتون و دو بیماری دیگر انجام دهند: مولتیپل اسکلروزیس پیشرونده اولیه (PPMS) و بیماری Pelizaeus-Merzbacher (PMD). اگرچه اکثر افراد مبتلا به ام اس، دوره های عود بیماری و پس از آن بهبودی دارند، اما حدود 15 درصد مبتلا به PPMS هستند که در آن این بیماری بدون دوره های بهبودی، کاملا بی وقفه پیشرفت می کند. PMD یک اختلال ژنتیکی نادر و پیشرونده است که به الیگودندروسیت ها آسیب می رساند و منجر به بدتر شدن هماهنگی، توانایی حرکتی و عملکرد مغزی بیمار می شود.
گلدمن گفت: ما هنوز باید از ایمنی طولانی مدت سلول ها پس از پیوند آنها کاملا مطمئن باشیم. اما ما انتظار داریم که این داده ها را در حدود دوسال دیگر با آزمایش های انسانی، تایید نهایی کنیم.