فهرست مطالب
بر اساس تحقیقات جدید، مشخص شده است که فعال کردن یک موج مغزی خاص از طریق نور و صوت درمانی، آزادسازی پپتیدها از نورونهای بیناعصاب افزایش را میدهد و باعث حذف پروتئینهای مرتبط با آلزایمر از طریق سیستم گلیمفاتیک مغز میشود.
به گزارش تکناک، تحقیقات جدید انجام شده توسط MIT و سایر موسسات، بهطور فزایندهای نشان میدهد که سوسو زدن نور و کلیک صدا در فرکانس ریتم گامای مغزی 40 هرتز ممکن است پیشرفت بیماری آلزایمر (AD) را کاهش دهد و علائم را هم در داوطلبان انسانی و هم در موشهای آزمایشگاهی، کاهش دهد.
در یک مطالعه جدید که در مجله Nature منتشر شده است، محققان با استفاده از موشهای آزمایشگاهی مبتلا به بیماری آلزایمر، مکانیسم کلیدی را نشان میدهند که ممکن است در پاکسازی پروتئینهای آمیلوئید که یکی از مشخصههای پاتولوژی بیماری آلزایمر است که از طریق سیستم گلیمفاتیک مغز که یک شبکه است که اخیراً به موازات رگهای خونی مغز کشف شده است، پخش میشود، نقش داشته باشد.
لیهوی تسای، نویسنده ارشد این مطالعه میگوید: از زمانی که اولین نتایج خود را در سال 2016 منتشر کردیم، مردم از من پرسیدند که این روش چگونه کار میکند؟ چرا 40 هرتز؟ چرا فرکانس دیگری نه؟ اینها واقعاً سؤالات بسیار مهمی هستند که ما در آزمایشگاه برای رسیدگی به آنها بسیار سخت کار کردهایم.
مقاله جدید مجموعهای از آزمایشها را توصیف میکند که توسط میچ مرداک زمانی که دانشجوی دکترای علوم شناختی و مغز در MIT بود، ارائه میشود و نشان میدهد که وقتی تحریک گامای حسی، قدرت 40 هرتز و همگامی را در مغز موشها افزایش میدهد، به نوع خاصی از نورونها را برای آزاد کردن پپتیدها فرمان میدهد.
نتایج بیشتر نشان میدهد که آن سیگنالهای پروتئینی کوتاه، فرآیندهای خاصی را هدایت میکنند که باعث افزایش پاکسازی آمیلوئید از طریق سیستم گلیمفاتیک میشوند.
مرداک گفت: ما هنوز نقشه خطی از توالی دقیق رویدادهایی که رخ می دهند، نداریم اما یافتههای آزمایشهای ما از این مسیر پاکسازی در مسیرهای اصلی گلیمفاتیک پشتیبانی میکنند.
01
از 02از گاما تا گلیمفاتیک
از آنجایی که تحقیقات قبلی نشان داده است که سیستم گلیمفاتیک، مجرای کلیدی برای پاکسازی ضایعات مغزی است و ممکن است توسط ریتمهای مغزی تنظیم شود، تسای و مرداک فرض کردند که این امر ممکن است به توضیح مشاهدات قبلی آزمایشگاه کمک کند که تحریک حسی گاما باعث کاهش میزان آمیلوئید در موشهای مبتلا به آلزایمر میشود.
هنگام آزمایش روی موشهای حامل ژن 5XFAD که بهطور ژنتیکی آلزایمر را شبیهسازی می کنند، مرداک و نویسندگان همکار ابتدا نتایج قبلی آزمایشگاه را تکرار کردند که نتایج از این قرار بود تحریک حسی 40 هرتز باعث افزایش فعالیت عصبی 40 هرتزی در مغز و کاهش میزان آمیلوئید میشود. سپس آنها تصمیم گرفتند تا اندازهگیری کنند که آیا هیچ تغییر مرتبطی در مایعاتی که از طریق سیستم گلیمفاتیک جریان مییابد تا مواد زائد را با خود حمل کنند، وجود دارد یا خیر. در واقع آنها افزایش مایع مغزی نخاعی را در بافت مغز موشهایی که تحت درمان با تحریک گامای حسی قرار گرفتهاند، در مقایسه با گروه تحت کنترل درماننشده، اندازهگیری کردند. آنها همچنین افزایش سرعت خروج مایع بینابینی از مغز را اندازهگیری کردند. علاوه بر این، در موشهای تحت درمان با گاما، مرداک افزایش قطر عروق لنفاوی که مایعات را تخلیه میکنند و افزایش تجمع آمیلوئید در غدد لنفاوی گردنی را اندازهگیری کرد، که محل تخلیه آن جریان است.
برای بررسی چگونگی وقوع این افزایش جریان مایع، محققان بر کانال آبی آکواپورین 4 (AQP4) سلولهای آستروسیت تمرکز کردند که سلولها را قادر میسازد تا تبادل مایع گلیمفاتیک را تسهیل کنند. هنگامی که آنها عملکرد APQ4 را با یک ماده شیمیایی مسدود کردند، از تحریک گامای حسی از کاهش سطوح آمیلوئید جلوگیری کرد و از بهبود یادگیری و حافظه موش جلوگیری کرد. محققان به عنوان یک آزمایش بیشتر از یک تکنیک ژنتیکی برای اختلال در AQP4 استفاده کردند، که در پاکسازی آمیلوئید مبتنی بر گاما تداخل داشت.
علاوه بر تبادل مایعی که توسط فعالیت APQ4 در آستروسیتها ایجاد میشود، مکانیسم دیگری که توسط آن امواج گاما جریان گلیمفاتیک را تقویت میکنند، افزایش ضربان عروق خونی همسایه است. چندین اندازهگیری، ضربانپذیری شریانی قویتری را در موشهایی که تحت تحریک گامای حسی قرار گرفتند در مقایسه با گروه تحت کنترل درمان نشده، نشان داد.
یکی از بهترین تکنیکهای جدید برای ردیابی اینکه چگونه یک وضعیت مانند تحریک گامای حسی، بر انواع سلولهای مختلف تأثیر میگذارد، توالیبندی RNA آنها برای ردیابی تغییرات در نحوه فعالیت ژنهایشان است. با استفاده از این روش، تسای و مرداک مشاهده کردند که تحریک حسی گاما در واقع تغییرات منطبق با افزایش فعالیت آستروسیت AQP4 را افزایش میدهد.
02
از 02تحریک توسط پپتیدها
دادههای توالییابی RNA نشان داد که با تحریک حسی گاما، زیرمجموعهای از نورونها به نام اینترنورونها افزایش قابلتوجهی در تولید چندین پپتید تجربه کردند. این مسئله تعجبآور نبود به این معنا که آزادسازی پپتید به فرکانسهای ریتم مغز وابسته است، اما همچنان قابل توجه بود زیرا یک پپتید ویژه، با مزایای مبارزه با آلزایمر مرتبط است و به تنظیم سلولهای عروقی، جریان خون و پاکسازی گلیمفاتیک کمک میکند.
با به دست آوردن این نتیجه جالب، محققان آزمایشهایی انجام دادند که نشان داد افزایش این پپتید ویژه در مغز موشهای تحت درمان با گاما وجود دارد. همچنین محققان از یک حسگر آزادسازی پپتید استفاده کردند و مشاهده کردند که تحریک گامای حسی منجر به افزایش آزادسازی پپتید از نورونهای فعالکننده ویژه میشود.
اما آیا این آزادسازی پپتید تحریک شده با گاما باعث پاکسازی گلمفاتیک آمیلوئید میشود؟ برای پی بردن به این موضوع، محققان آزمایش دیگری انجام دادند. آنها نورونهای ویژه را به صورت شیمیایی خاموش کردند. هنگامی که آنها این کار را انجام دادند و سپس موشها را در معرض تحریک گامای حسی قرار دادند، به این نتیجه رسیدند که دیگر افزایشی در ضربانپذیری شریانی وجود ندارد و دیگر پاکسازی آمیلوئید تحریک شده با گاما وجود ندارد.
مرداک گفت: ما فکر میکنیم که نوروپپتیدهای زیادی در این شرایط درگیر هستند. تسای افزود که یک جهت جدید اصلی برای تحقیقات آزمایشگاهی، تعیین اینکه چه پپتیدهای دیگر یا سایر عوامل مولکولی ممکن است توسط تحریک گامای حسی هدایت شوند، خواهد بود.
تسای و مرداک افزودند که اگرچه این مقاله بر روی مکانیسم مهمی به نام پاکسازی گلیمفاتیک آمیلوئید متمرکز است که توسط آن تحریک گامای حسی به مغز کمک می کند، احتمالاً این تنها مکانیسم اساسی نیست که مهم است. در این مطالعه اثرات پاکسازی نسبتاً سریع اتفاق افتاد، اما در آزمایشها و مطالعات بالینی، به هفتهها یا ماهها برای تحریک مزمن گامای حسی برای داشتن اثرات پایدار بر شناخت مورد نیاز بوده است.
دانشمندان با تحقیقات بیشتر در مورد اینکه چگونه تحریک حسی ریتم مغز ممکن است به درمان اختلالات عصبی کمک کند، میآموزند.
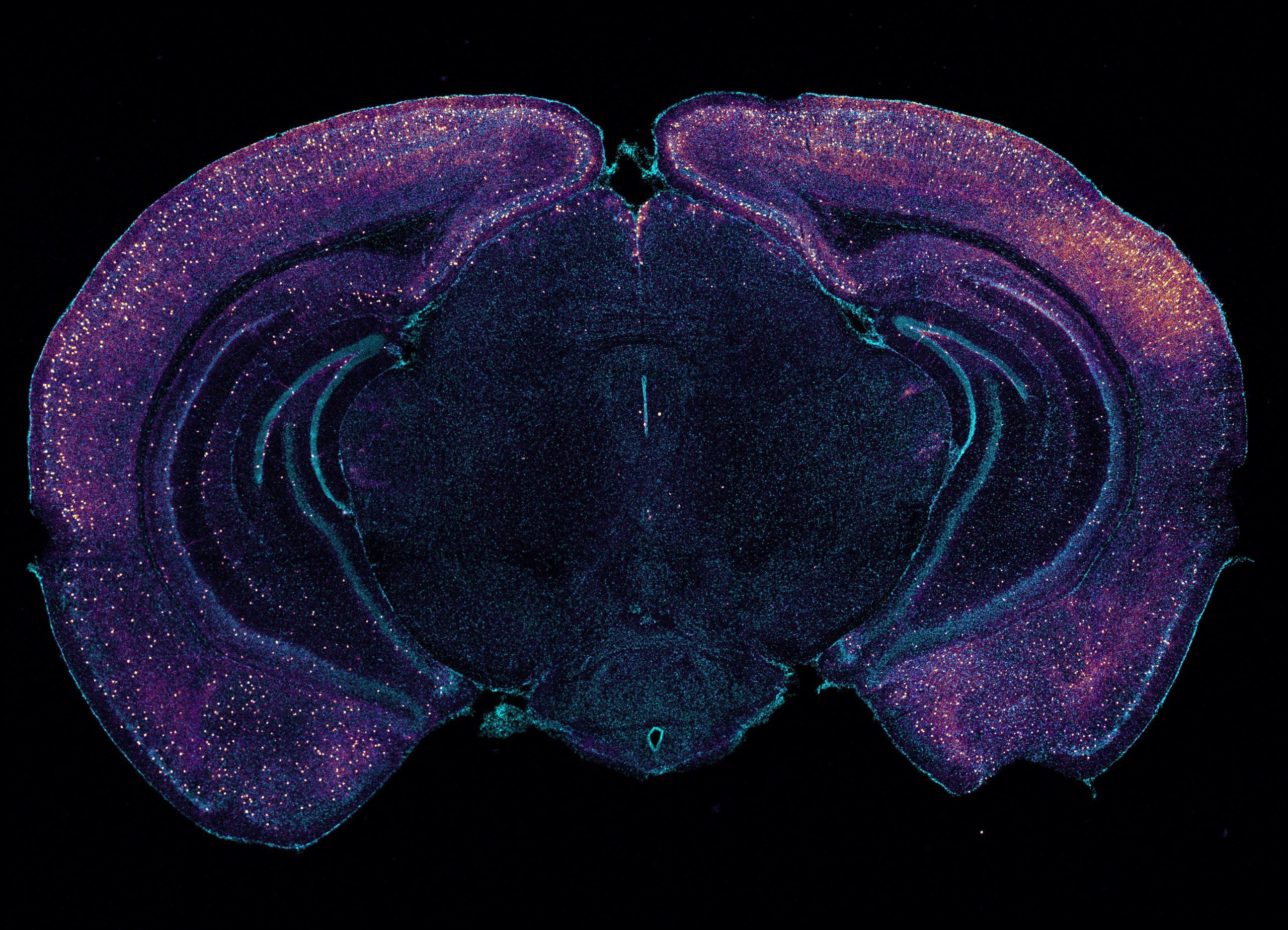
(زیرنویس تصویر: رنگآمیزی روشن نشاندهنده نورونهای فعالکننده ویژه در این مقطع تاجی مغز موش هستند. نورونها ممکن است از طریق آزادسازی پپتیدها به پاکسازی گلیمفاتیک آمیلوئید کمک کنند)