یک روش جدید (اپتوژنتیک )با هدف قرار دادن نورون های بیمار در مغز و تغییر رفتار طولانی مدت آنها با استفاده از نور درمان های موثری را برای بیماری های عصبی مانند صرع و اوتیسم ایجاد کرده است.
به گزارش تکناک، ، این روش درمانی توسط محققان دانشکده مهندسی هاروارد جان A. Paulson و علوم کاربردی (SEAS) و MIT ایجاد شده است.
جیا لیو،استادیار مهندسی زیستی در موسسه SEAS و نویسنده ارشد این مطالعه گفت: ما تصور می کنیم که این فناوری فرصت های جدیدی را برای کنترل وضوح مکانی-زمانی بالای نورون ها برای مطالعات علوم اعصاب و رفتار و توسعه درمان های جدید برای اختلالات عصبی فراهم می کند.
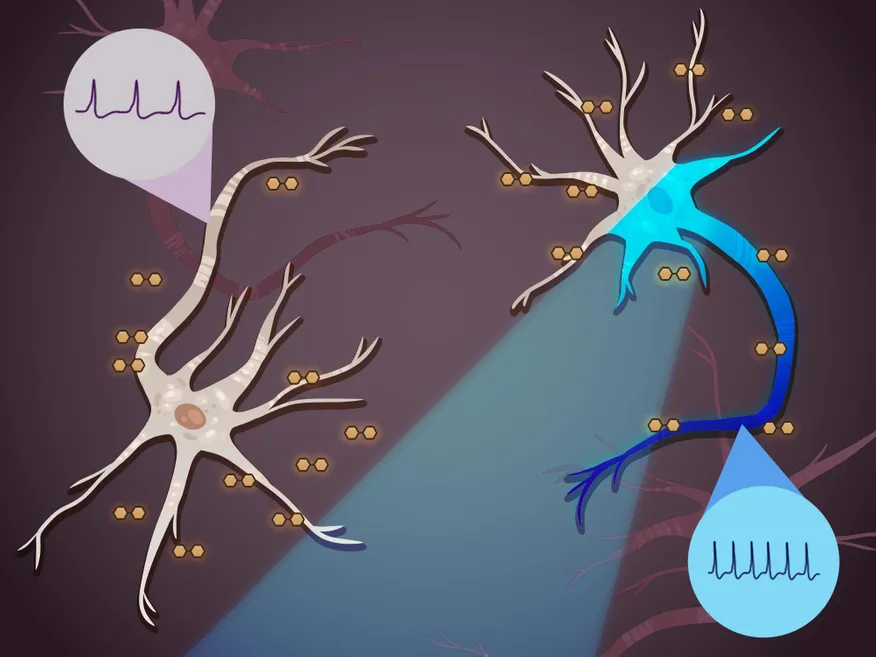
اپتوژنتیک روشی است که با استفاده از نور برای تحریک یا مهار نورونها،مدتهاست که نوید تحولی شگرف در مطالعه و درمان بیماریهای عصبی که ناشی از تحریکپذیری بیش از حد یا ضعیف نورونها است را می دهد.با این حال، تکنیکهای اپتوژنتیک فعلی تنها میتوانند تحریکپذیری نورونها را در کوتاهمدت تغییر دهند. هنگامی که نور خاموش می شود،نورون ها به رفتار اصلی خود باز می گردند.
پیشرفتهای اخیر در فناوری نانو،از جمله نانوالکترونیک قابل کاشت و انعطافپذیر که توسط لیو و تیمش رقم خورده،میتواند رفتار عصبی را در درازمدت تغییر دهد،اما این دستگاهها باید در مغز کاشته شوند و نمیتوان آنها را برای هدف قرار دادن نورونهای خاص درگیر در مغز برنامهریزی کرد.
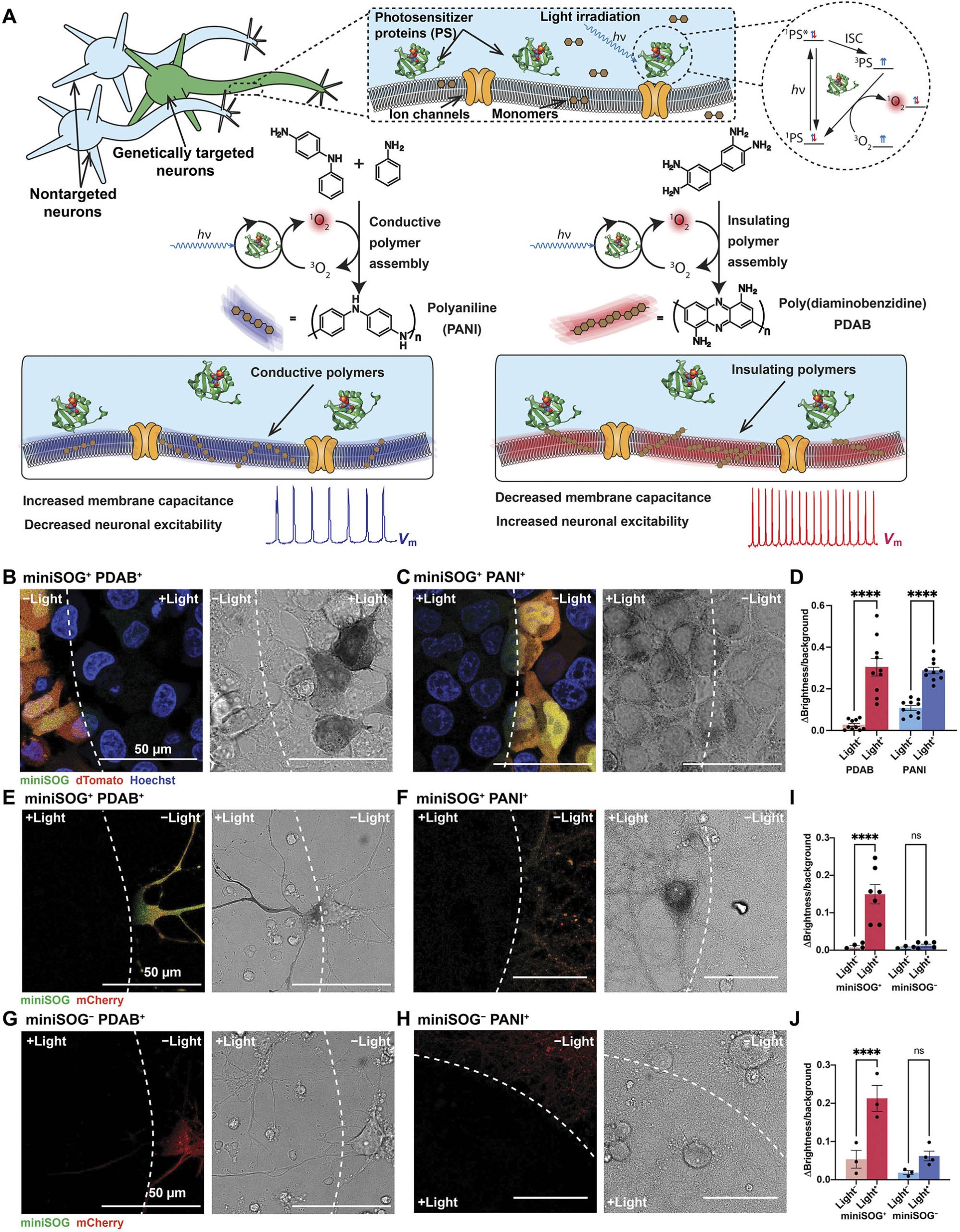
تحریک پذیری یک نورون توسط دو جزء اصلی کنترل می شود:رسانایی کانال یونی آن و توانایی غشای سلولی برای ذخیره بار الکتریکی که به عنوان ظرفیت آن شناخته می شود.
بیشتر تکنیکهای اپتوژنتیک هدایت کانال یونی را هدف قرار میدهند و با باز کردن یا بستن گروه خاصی از کانالها،تحریکپذیری نورون را تعدیل میکنند.این رویکرد می تواند به طور موثر تحریک پذیری نورون را تنظیم کند،اما فقط به صورت گذرا.
لیو گفت: شما می توانید یک نورون را به عنوان یک مدار مقاومت-خازن و غشای سلولی را به عنوان یک ماده دی الکتریک تصور کنید.درست مانند هر مدار دیگری، اگر ظرفیت ماده که در این مورد غشای سلولی است،را تغییر دهید،می توانید تحریک پذیری ذاتی مدار را در دراز مدت،از تحریک پذیری بالا به تحریک پذیری کم یا بالعکس تغییر دهید.
برای تغییر ظرفیت غشای سلولی، لیو، با همکاری شیائو وانگ، توماس دی و استادیار شیمی کابین ویرجینیا در موسسه MIT، از آنزیمهای حساس به نور استفاده کرد که میتوانند باعث تشکیل پلیمرهای عایق یا رسانا بر روی سطح غشای سلولی شوند.
آنزیم ها را می توان برای هدف قرار دادن غشای سلولی نورون های خاص مهندسی کرد.هنگامی که آنزیم ها به غشای مشخص شده متصل شدند،محققان از نور آبی برای روشن کردن نورون ها استفاده کردند که باعث تولید پوشش های عایق یا رسانا بر روی غشاء در عرض چند دقیقه شد.آنها نشان دادند که نورونهای دارای پوششهای پلیمری عایق تحریکپذیرتر شدند و نورونهایی با پوششهای پلیمری رسانا کمتر تحریکپذیر شدند.
محققان متوجه شدند که میتوانند با نحوه قرار گرفتن در معرض نور، تحریکپذیری را تنظیم کنند.هر چه نورونها بیشتر در معرض نور قرار گیرند،پوششها عایقتر یا رساناتر میشوند.تیم تحقیقاتی همچنین نشان داد که تغییرات در تحریک پذیری تا سه روز ادامه دارد.در حقیقت این تغییرات تا زمانی که دانشمندان بتوانند نورون ها را در یک ظرف پتری زنده نگه دارند،ادامه خواهد داشت.
در مرحله بعد،تیم قصد دارد این رویکرد را با استفاده از برش هایی از بافت مغز و در حیوانات آزمایش کند.
لیو در آخر افزود: هدف کلی این کار، فعال کردن رویکردهایی برای تغییر الگو ادغام مواد،ساختارها و دستگاه های کاربردی در سیستم های عصبی زنده با ویژگی های درون سلولی منحصر به فرد است که امکان دستکاری دقیق خواص الکتروشیمیایی درون سلولی یعنی بازسازی تحریک پذیری نورون ها در سیستم های عصبی زنده را فراهم می کند.