محققان دانشگاه پیتسبورگ، نانوذرات ضد سرطانی تولید کرده اند که به طور همزمان شیمی درمانی و ایمونوتراپی جدیدی را ارائه می دهند.
به گزارش تکناک، دکتر سونگ لی نویسنده ارشد این تحقیق گفت: کشف یک هدف درمانی و یک حامل نانویی جدید برای تاثیر بیشتر ایمونوتراپی و داروهای شیمی درمانی دو جنبه نوآورانه این مطالعه محسوب می شود.
من در مورد این تحقیق بسیار هیجان زده هستم زیرا بنظر می رسد که کاربرد زیادی داشته باشد.ما هنوز نمی دانیم که آیا این رویکرد جدید در بیماران موثر است یا خیر، اما یافته های ما نشان می دهد که این نوع درمان پتانسیل زیادی برای استفاده دارد.
شیمی درمانی یکی از ستون های درمان سرطان است،اما سلول های سرطانی باقی مانده می توانند در بدن بمانند و باعث عود تومور سرطانی شوند.در این فرآیند لیپیدی به نام فسفاتیدیل سرین (PS) وجود دارد که معمولاً در داخل لایه داخلی غشای سلول تومور یافت می شود اما در مواجه با داروهای شیمی درمانی به سطح سلول مهاجرت می کند.در سطح سلول، PS به عنوان یک سرکوب کننده ایمنی عمل می کند و سلول های سرطانی باقی مانده را در مقابل سیستم ایمنی محافظت می کند.

محققان دانشگاه پیت متوجه شدند که درمان توسط داروهای شیمی درمانی فلوئورواوراسیل و اکسوپلاتین (FuOXP) منجر به افزایش سطح Xkr8 که پروتئینی است که توزیع PS را روی غشای سلولی کنترل می کند،می شود.این یافته نشان میدهد که مسدود کردن Xkr8 از انتقال سلولهای سرطانی به سطح سلولی PS جلوگیری میکند و به سلولهای ایمنی اجازه میدهد تا سلولهای سرطانی باقیمانده پس از شیمیدرمانی را پاک کنند.
در یک مطالعه مستقل که اخیراً در Cell Reports منتشر شد،دکتر یی نان گونگ، استادیار ایمونولوژی در دانشگاه پیت، Xkr8 را به عنوان یک هدف درمانی جدید برای تقویت پاسخ ایمنی ضد تومور شناسایی کرد.
لی و تیمش تکههایی از کد ژنتیکی به نام RNA تداخل کوتاه (siRNA) طراحی کردند که تولید پروتئینهای خاص که در این مورد Xkr8 است را متوقف میکند.پس از بسته بندی siRNA و FuOXP با هم در نانوذرات دوعملی، مرحله بعدی هدف قرار دادن آنها به سمت تومورها بود.

نانوذرات ها معمولاً برای عبور از رگهای خونی دستنخورده در بافت سالم بسیار بزرگ هستند،اما میتوانند به سلولهای سرطانی برسند،زیرا تومورها گاهی رگهای ضعیفی دارند که با سوراخهایی که دارند به آنها اجازه عبور میدهد.اما این هدف گیری تومور محدود است زیرا بسیاری از تومورهای انسانی سوراخ های کافی برای عبور نانوذرات را ندارند.
لی گفت: مانند یک کشتی که مردم را از یک طرف رودخانه به سمت دیگر می برد،ما می خواستیم مکانیزمی ایجاد کنیم که به نانوذرات اجازه می دهد بدون اتکا به سوراخ ها از رگ های خونی دست نخورده عبور کنند.
برای توسعه چنین کشتی،محققان سطح نانوذرات را با کندرویتین سولفات و PEG تزئین کردند.این ترکیبات به نانوذرات کمک میکنند تا تومورها را هدف قرار دهند و با اتصال به گیرندههای سلولی مشترک در رگهای خونی تومور و سلولهای تومور و طولانیتر کردن مدت زمان ماندن آنها در جریان خون در بافت سالم جلوگیری کنند.
هنگامی که این دارو به موش تزریق شد،حدود 10 درصد از نانوذرات راه خود را به تومور خود رساندند که این میزان نشان دهنده ی پیشرفت قابل توجهی نسبت به سایر پلتفرم های نانوحامل است. .تجزیه و تحلیل در تحقیقات منتشر شده قبلی نشان داد که به طور متوسط تنها 0.7 درصد از دوزهای نانوذرات به هدف خود می رسند.
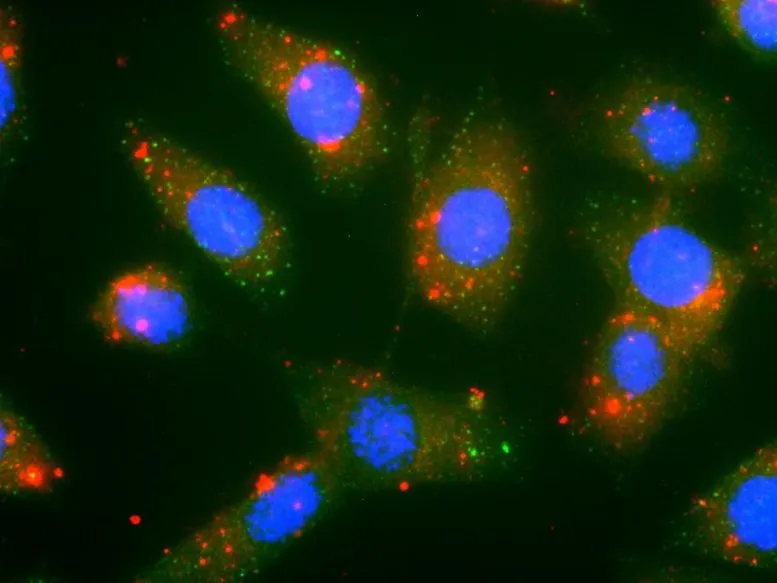
نانوذرات با عمل دوگانه به تنهایی به طور چشمگیری مهاجرت PS سرکوب کننده سیستم ایمنی به سطح سلول را در مقایسه با نانوذرات حاوی داروی شیمیایی FuOXP کاهش داد.
سپس، محققان پلتفرم خود را در نمونه های موش مبتلا به سرطان روده بزرگ و پانکراس آزمایش کردند. حیواناتی که توسط نانوذرات حاوی هر دو FuOXP و siRNA درمان شده بودند،نسبت به حیواناتی که دوزهای دارونما یا FuOXP دریافت کردهاند،ریزمحیطهای توموری بهتر به همراه سلولهای T بیشتر و میزان کمتری از سلولهای T تنظیمکننده سرکوبکننده ایمنی داشتند.
در نتیجه،موشهایی که نانوذرات siRNA-FuOXP را دریافت کردند،کاهش چشمگیری در اندازه تومور در مقایسه با حیواناتی که تنها یک درمان را دریافت کردند،نشان دادند.
به گفته لی،این مطالعه همچنین به پتانسیل ترکیب نانوذرات FuOXP-siRNA با نوع دیگری از ایمونوتراپی به نام بازدارندههای نقطه کنترل اشاره کرد. نقاط بازرسی ایمنی مثل PD-1 مانند ترمز بر روی سیستم ایمنی عمل می کنند،اما مهارکننده های ایست بازرسی با آزاد کردن ترمزها و کمک به سلول های ایمنی برای مبارزه با سرطان کار می کنند.
محققان متوجه شدند که نانوذرات FuOXP با وجود یا عدم وجود siRNA باعث افزایش میزان PD-1 می شود. اما زمانی که آنها یک داروی مهارکننده PD-1 را اضافه کردند،درمان ترکیبی پیشرفت های چشمگیری در رشد و بقای تومور در موش ها داشت.
این تیم با توجه به اینکه قصد دارد درمان جدید خود را به جامعه ارائه کند،اکنون به دنبال تأیید یافته های خود با آزمایش ها و ارزیابی بیشتر برای بررسی عوارض جانبی بالقوه هستند.























