فهرست مطالب
در مطالعهای که اخیراً در مجله Cell Reports منتشر شده است، محققی به نام دکتر جرولد چون و گروه تحقیقاتیاش به این نتیجه رسیدند که دستورالعملهای مولکولی موجود در وزیکولها در میان نمونههای مغز پس از مرگ افراد مبتلا به بیماری آلزایمر، بسیار متفاوت است.
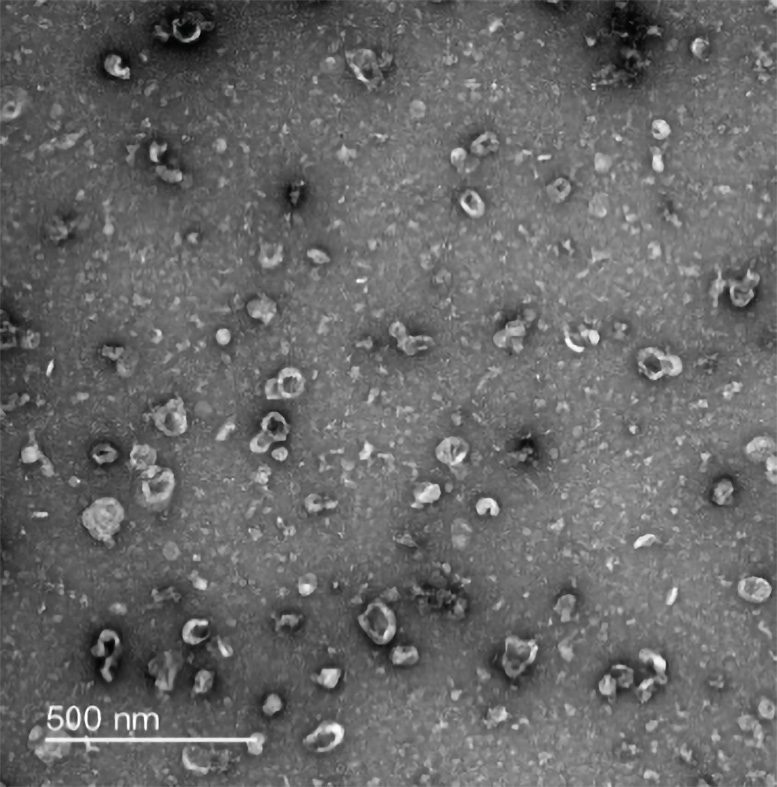
به گزارش تکناک، محققان در این مطالعه حبابهای کوچک مغزی را که تحت بررسی قرار گرفتهاند، وزیکولهای خارج سلولی کوچک (sEVs) مینامند. این بادکنکهای آب بیولوژیکی کوچک توسط اکثر سلولهای بدن تولید میشوند تا طیف گستردهای از پروتئینها، لیپیدها و محصولات جانبی متابولیسم سلولی و همچنین کدهای اسید نوکلئیک RNA را که توسط سلولهای گیرنده برای ساخت پروتئینهای جدید استفاده میشود، منتقل کنند.
از آنجایی که این محموله فعال بیولوژیکی میتواند به راحتی تغییراتی را در سلولهای دیگر ایجاد کند، دانشمندان علاقهمند به بررسی وزیکولهای خارج سلولی کوچک مغز بهعنوان وسیلهای برای عبور از امتداد دستورالعملهای معمولی و همچنین بههمپیوسته برای پروتئینهای نادرست تا شده که با پیشرفت بیماریهای تخریبکننده عصبی مانند بیماری آلزایمر در مغز انباشته میشوند، بودند.
برای اینکه وزیکول خارج سلولی کوچک نقش بالقوهای در ایجاد پروتئینهای ناخواسته داشته باشد، باید نقشههایی با اطلاعات کافی داشته باشد تا سلولهای دیگر را قادر به تولید پروتئینهای مشکلساز کند. اکثر تحقیقات قبلی نشان داده بودند که نقشههای حامل RNA پیامرسان (mRNA) برای پروتئینها به قطعات بسیار کوتاهتری خرد میشوند تا به سلولهای گیرنده اجازه دهند الگوهای ساخت خود را تغییر دهند.
چون میگوید: ما در مطالعه خود متوجه شدیم که این موضوع کاملاً برعکس است. ما بیش از 10000 mRNA تمام قد را با استفاده از تکنیک توالییابی DNA نسبتا جدیدی به نام توالی خوانی طولانی مدت PacBio شناسایی کردیم.
01
از 01یافتههای تفصیلی تحقیق
محققان وزیکولهای خارج سلولی را از قشر جلوی مغز اهدایی 12 بیمار پس از مرگ که مبتلا به بیماری آلزایمر بودند و 12 نمونه از اهداکنندگان بدون بیماری آلزایمر (یا هر بیماری عصبی شناخته شده دیگری) جدا کردند.
تقریباً 80 درصد از mRNA های شناسایی شده تمام طول خود را حفظ کرده بودند که این مسئله به آنها اجازه میداد توسط سلولهای گیرنده به پروتئینهای زنده رونویسی شوند.
نویسنده اول این مطالعه، دکتر لینیا رانسوم میگوید: برای تأیید نتایج توالییابی طولانی مدت در نمونههای انسانی، ما وزیکولهای جدا شده از سلولهای موش را نیز بررسی کردیم. ما میانگینهای مشابهی بین 78 تا 86 درصد رونوشتهای تمام قد را در سه نوع سلول مغزی یافتیم: آستروسیتها، میکروگلیا و نورونها.
محققان علاوه بر تجزیه و تحلیل و تایید نتایج مربوط به طول mRNA ها در وزیکولهای خارج سلولی مغز، توالی ژنهای منعکس شده در رونوشت وزیکولهای خارج سلولی mRNA را مقایسه کردند. در نمونههای مبتلا به بیماری آلزایمر، 700 ژن افزایش فعالیت داشتند در حالی که تقریباً 1500 ژن کاهش فعالیت داشتند.
دانشمندان به این نتیجه رسیدند که 700 ژن تنظیمشده، با التهاب و فعالسازی سیستم ایمنی مرتبط هستند که این یافته با الگوهای شناختهشده التهاب مغزی موجود در بیماریهای تخریبکننده عصبی مانند بیماری آلزایمر مطابقت دارد. همچنین محققان کشف کردند که بسیاری از ژنهای مرتبط با بیماری آلزایمر در مطالعات قبلی مرتبط با وزیکولهای خارج سلولی ژنوم در بیماری آلزایمر نیز وجود داشتند.
چون میگوید: تغییرات در فعالیت ژن موجود در این وزیکولها نشانهای از التهاب است که ممکن است دریچهای به فرآیندهای بیماری باشد که در مغز با پیشرفت بیماری آلزایمر اتفاق میافتد.
پس از این مطالعه، چون و گروهش به بررسی عمیقتر چگونگی بستهبندی سلولهای و وزیکولهای خارج سلولی و اینکه چگونه کدهای mRNA محصور شده منجر به تغییرات عملکردی در سایر سلولهای مغزی مبتلا به بیماری آلزایمر میشوند، خواهند پرداخت.
درک بهتر وزیکولهای خارج سلولی و محتویات mRNA آنها ممکن است کشف نشانگرهای زیستی را امکان پذیر کند که میتوانند به منظور بهبود تشخیص زودهنگام بیماری آلزایمر و سایر بیماریهای عصبی مورد استفاده قرار گیرند، در حالی که مکانیسمهای بیماری جدید را برای ارائه اهداف درمانی جدید شناسایی میکنند.
چون میگوید: وزیکولهای خارج سلولی بهطور طبیعی بهعنوان وسیلهای برای انتقال محمولههای فعال بیولوژیکی بین سلولها ظاهر میشوند، بنابراین ممکن است در آینده بتوان از آنها به عنوان یک سیستم تحویل هدفمند درمانی برای درمان بیماریهای مغزی استفاده کرد.