فهرست مطالب
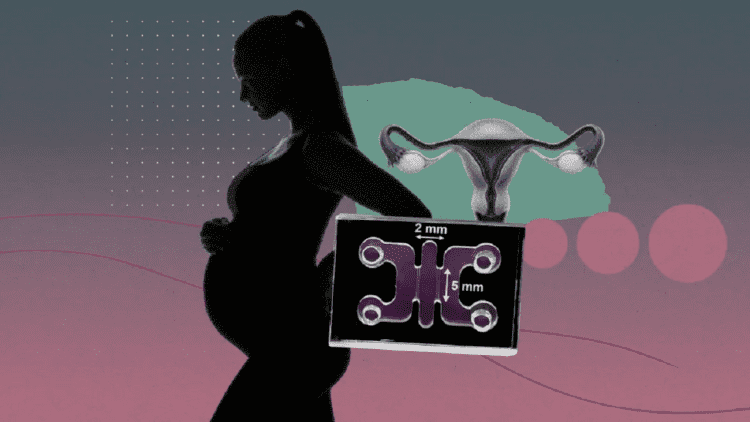
محققان در چین با استفاده از ارگانوئید رحم و جنینهای آزمایشگاهی توانستهاند مراحل ابتدایی کاشت جنین را شبیهسازی کنند.
به گزارش سرویس علمی تکناک، در نگاه اول، صحنه شبیه آغاز یک بارداری انسانی است، اما نکته شگفتانگیز این است که هیچ یک از این فرایندها در بدن انسان رخ نمیدهد. تصاویر در آزمایشگاهی در پکن و داخل یک تراشه میکروفلوئیدیک ثبت شدهاند.
در سه مقالهای که این هفته توسط Cell Press منتشر شد، پژوهشگران از این دستاورد به عنوان دقیقترین تلاشها برای شبیهسازی لحظات ابتدایی بارداری در آزمایشگاه یاد کردهاند. در این مطالعات، جنینهای انسانی از مراکز IVF گرفته شدهاند و با «ارگانوئید»هایی (اندامواره) ساختهشده از سلولهای اندومتر ترکیب شدهاند، که پوشش داخلی رحم را تشکیل میدهند. دو گزارش از چین و یک گزارش بینالمللی با مشارکت پژوهشگرانی از بریتانیا، اسپانیا و آمریکا نشان میدهد که دانشمندان چگونه از بافتهای مهندسیشده برای درک دقیقتر مراحل ابتدایی بارداری و بهبود نتایج IVF استفاده میکنند.
حتما بخوانید: اولین تصاویر سهبعدی لانهگزینی جنین انسان ثبت شد!
01
از 03فرایند لقاح مصنوعی
جون وو، زیستشناس دانشگاه تگزاس Southwestern Medical Center در دالاس که در هر دو گزارش چینی مشارکت داشته است، بیان کرد: «شما جنین و ارگانوئید اندومتر را با هم دارید. این پیام کلی هر سه مقاله است.» بر اساس این مقالات، این ترکیبهای سهبعدی کاملترین بازآفرینی از نخستین روزهای بارداری تاکنون هستند و میتوانند در مطالعه دلایل ناکامیهای متداول IVF کاربردی باشند. در تمامی آزمایشها، زمانی که جنینها به دو هفته رسیدند (یا زودتر)، آزمایش متوقف شد؛ محدودیتی ناشی از قوانین حقوقی و ملاحظات اخلاقی که معمولا دانشمندان را از ادامه تحقیقات بیش از ۱۴ روز منع میکنند. در روند استاندارد IVF، تخمک در آزمایشگاه بارور و به جنینی کروی به نام بلاستوسیت تبدیل میشود؛ این فرایند چند روز طول میکشد. سپس بلاستوسیت به رحم بیمار منتقل میشود تا بتواند در آنجا مستقر گردد و در نهایت به نوزادی سالم تبدیل شود.
بیشتر بخوانید: اولین نوزاد از طریق رحم پیوندی در بریتانیا متولد شد

یکی از نقاط ضعف رایج در درمان IVF این است که بسیاری از بیماران متوجه میشوند که فرایند موفق نبوده است، چرا که جنین هرگز به رحم نمیچسبد. در گزارشهای جدید، همان اتصال ابتدایی بین مادر و جنین در محیط آزمایشگاهی بازسازی شده است. ماتئو مول، زیستشناس دانشگاه استنفورد که نتایج آن همراه با همکاران اروپایی، امروز منتشر شده است، توضیح داد: «IVF به معنای لقاح آزمایشگاهی است، اما اکنون این مرحله لقاح آزمایشگاهی نیست، بلکه مرحله شبیهسازی کاشت جنین است. اگر بتوانیم آن را در آزمایشگاه مدلسازی کنیم، پتانسیل افزایش نرخ موفقیت وجود دارد.» هونگمی وانگ، زیستشناس در موسسه سلولهای بنیادی و پزشکی بازساختی پکن و از رهبران این پروژه گفت: «به طور معمول مرحله کاشت کاملا از دید پنهان است، چرا که در رحم فرد رخ میدهد.» وانگ معمولا روی میمونها مطالعه میکند، چرا که میتواند بارداری آنها را متوقف کنند و بافتهای مورد نیاز خود را جمعآوری نماید. وی تصریح کرد: «همیشه امیدوار بودیم که بتوانیم کاشت جنین انسانی را درک کنیم، اما راهی برای این کار نداشتیم؛ همه چیز در رحم اتفاق میافتد.»
در مطالعه پکن، پژوهشگران حدود ۵۰ جنین اهدایی IVF را مورد آزمایش قرار دادند و هزار آزمایش دیگر با استفاده از بلاستوییدها انجام شد. بلاستوییدها شبیهسازهای جنین انسان در مراحل اولیه هستند که از سلولهای بنیادی ساخته شدهاند. این بلاستوییدها به راحتی در حجم زیاد تولید میشوند و از آنجایی که جنین واقعی نیستند، محدودیتهای اخلاقی کمتری در استفاده از آنها اعمال میشود. لقیان یو، نویسنده ارشد گزارش عنوان کرد: «سوال این بود که اگر این بلاستوییدها را داریم، چه کاربردی میتوانند داشته باشند؟ گام واضح بعدی، کاشت بود. پس چگونه این کار را انجام دهیم؟» برای تیم پکن، راهکار ساخت یک محفظه نرم سیلیکونی با کانالهای ریز بود تا بتوانند مواد مغذی را وارد و فضایی برای رشد ارگانوئید رحم فراهم کنند. پس از آمادهسازی، بلاستوییدها (یا جنینهای واقعی) میتوانند از طریق یک پنجره کوچک در دستگاه وارد شوند و فرایند «بارداری آزمایشگاهی» آغاز شود.
برای مطالعه بیشتر: تولد شگفتانگیز نوزاد آمریکایی از جنین ۳۱ ساله منجمد
02
از 03رشد ارگانوئید رحم
لقیان یو، نویسنده ارشد گفت: «سوال کلیدی ما این است که نخستین ارتباط بین جنین و مادر چگونه شکل میگیرد. فکر میکنم این شاید اولین باری باشد که میتوانیم کل این فرایند را به طور کامل مشاهده کنیم.» پزشکان برای انجام شبیهسازی کاشت جنین در آزمایشگاه، ابتدا یک نمونهبرداری از پوشش رحم بیمار تهیه میکنند و از آن ارگانوئیدهای رحم را رشد میدهند. سپس بلاستوییدها به این ارگانوئیدها اضافه میشوند تا مشخص شود که زن قادر به حمایت از بارداری خواهد بود یا خیر. اگر بلاستوییدها شروع به کاشت نکنند، این ممکن است نشاندهنده عدم پذیرش رحم بیمار و علت شکست IVF باشد.

همچنین تیم پکن معتقد است که ارگانوئیدهای بارداری میتوانند برای شناسایی داروهایی که ممکن است به بیماران کمک کنند، مورد استفاده قرار گیرند. آنها در مقاله خود شرح دادهاند که چگونه از بافت زنان با سابقه شکستهای مکرر IVF ارگانوئید ساختند و سپس ۱،۱۱۹ داروی تاییدشده را روی این نمونهها آزمایش کردند تا تاثیر هر یک را بررسی کنند. چند دارو نتایج امیدوارکنندهای داشتند. یکی از این مواد، آوو بنزون، که در برخی کرمهای ضدآفتاب یافت میشود، شانس کاشت بلاستویید را از ۵ درصد به حدود ۲۵ درصد افزایش داد. یو اعلام کرده که مرکز او امیدوار است در آینده، در صورت یافتن داروی مناسب، یک آزمایش بالینی را آغاز کند.
03
از 03کاربردهای پزشکی شبیهسازی کاشت جنین
تیم پکن در حال بهبود سیستم ارگانوئید است تا واقعگرایانهتر شود. در وضعیت فعلی، این سیستم فاقد سلولهای کلیدی مانند سلولهای ایمنی و تامین خون است. یو توضیح داد که گام بعدی او افزودن رگهای خونی و پمپهای مینیاتوری به دستگاه چیپ است تا ارگانوئیدها بتوانند نوعی گردش خون ابتدایی داشته باشند. این یعنی در آینده نزدیک، به احتمال زیاد بلاستوییدها یا جنینها میتوانند مدت طولانیتری در آزمایشگاه رشد کنند و این پرسش مطرح میشود که دانشمندان تا چه حد قادر به ادامه بارداری در شرایط آزمایشگاهی خواهند بود. وو بیان کرد: «فناوری فعلی این امکان را ایجاد میکند که رشد طولانیتر را مشاهده کنیم.»
برخی پژوهشگران این پروژه را گامی نخستین برای پرورش نوزادان خارج از بدن میدانند. با وجود این، وو تاکید کرد که پرورش کامل انسان تا زمان تولد در آزمایشگاه در حال حاضر غیرممکن است. او گفت: «این فناوری به طور قطع با اکتوژنسیس، یعنی رشد خارج از بدن مرتبط است، اما هنوز هیچ شباهتی به رحم مصنوعی ندارد و این حوزه همچنان در قلمرو علمی-تخیلی قرار دارد.»