فهرست مطالب
پژوهشی جدید نشان میدهد که بیماری مالتیپل اسکلروزیس یا اماس ممکن است یک بیماری واحد نباشد، بلکه حاصل دو مسیر زیستی متفاوت باشد.
به گزارش سرویس علمی تکناک، بیماری اماس برای سالها بیشتر بر مبنای علائم بالینی تعریف شده و به زیستشناسی مولد آن توجه نشده است. اکنون این مطالعه تازه این چارچوب را به چالش میکشد، که میتواند برداشت بالینی از تشخیص، دینامیک پیشرفت بیماری و استراتژیهای درمانی را بازآرایی کند.
حتما بخوانید: مدل هوش مصنوعی JETS؛ الگوی جدید پیشبینی بیماری با دادههای اپل واچ
01
از 02روند درمان بیماری اماس
در تشخیص بالینی، اماس همچنان به عنوان یک بیماری واحد با دامنهای گسترده از علائم، مدیریت میشود. تصمیمهای درمانی بر اساس الگوهای التهاب، تغییرات تصویربرداری و نشانههای عصبی اتخاذ میشوند. با وجود این، ناهمگنی پاسخ درمانی و سیر پیشرفت، چالشی مزمن باقی مانده است؛ داروهایی که برای گروهی موثر هستند، برای گروهی دیگر ناکام میمانند و پیشرفت بیماری اغلب از چارچوبهای استاندارد سرپیچی میکند. مطالعهای که در نشریه Brain منتشر شده است، بیان میکند که این ناهمگنی شاید بازتاب وجود بیش از یک الگوی زیستی پایهای باشد. به بیان دیگر، آنچه به عنوان تنوع درون یک اختلال تلقی میشد، ممکن است ناشی از مسیرهای متفاوت نورودژنراسیون باشد.
بیشتر بخوانید: تراشههای بیوالکترونیکی MIT؛ درمان بیماریهای عصبی بدون جراحی
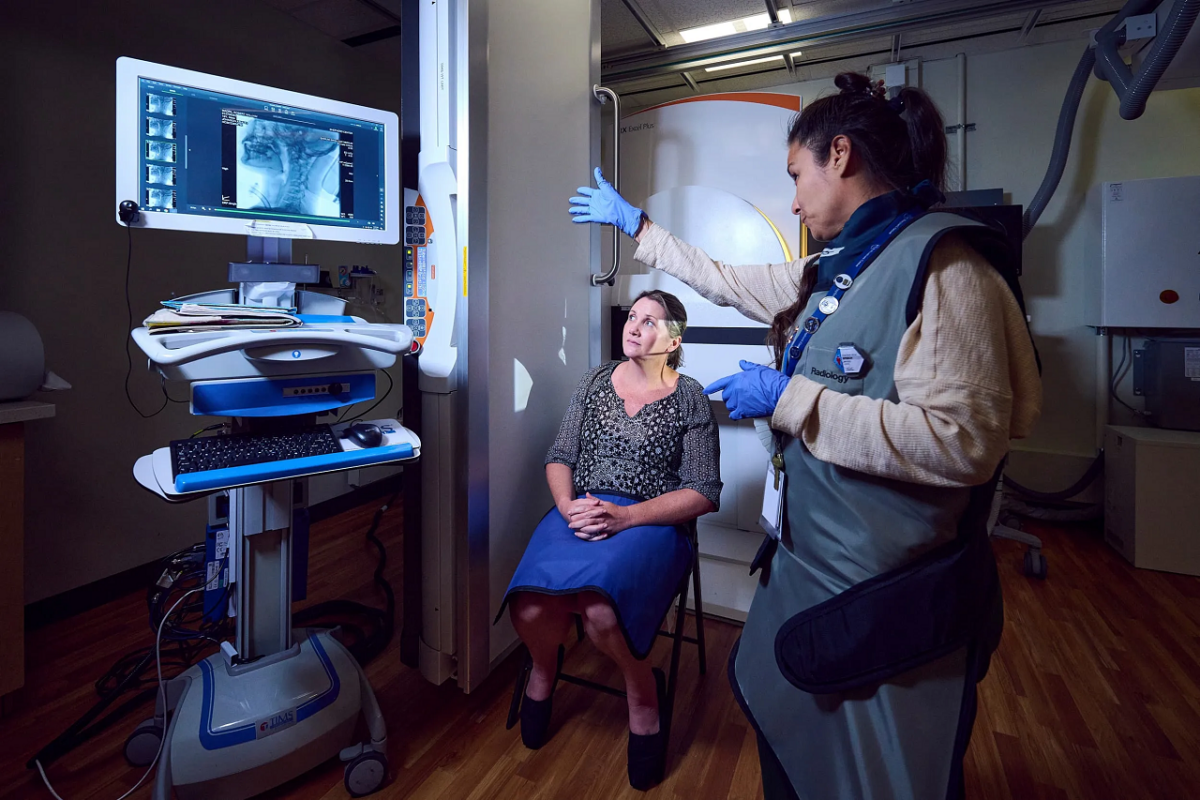
برای آزمون این ایده، تیمی از پژوهشگران در دانشگاه کالج لندن و Queen Square Analytics تمرکز را از علائم بالینی به سیگنالهای زیستی آسیب مغزی معطوف کردند. آنها با هدف شناسایی الگوهای پنهان تخریب بیماری اماس، دو منبع داده مکمل را ادغام کردند، که شامل نشانگر خونی sNfL به عنوان شاخص آسیب آکسونی و MRIهای سریالی برای ترسیم گسترش تخریب ساختاری در مغز بودند. تحلیل همزمان این دادهها با استفاده از سامانه یادگیری ماشین SuStaIn انجام شد؛ مدلی که برای کشف زیرگونهها و ترسیم مراحل پیشرفت بیماری طراحی شده است. نتایج حاصل از دادههای ۶۳۴ بیمار نشان داد که بهجای یک مسیر زیستی یکنواخت، دو الگوی ساختاری مجزا شامل درگیری زودرس قشر مغز و تخریب غالب ماده سفید وجود دارد.
برای مطالعه بیشتر: کشف یک نوع متمایز و جدید از بیماری دیابت
02
از 02اعتبارسنجی یافتهها
این دو زیرگونه نهتنها از نظر توپوگرافی آسیب متفاوت بودند، بلکه ریتم پیشرفت متمایزی نیز داشتند؛ یکی سیر کندتر و دیگری نورودژنراسیون شتابانتری داشت. چنین شکافی میتواند این موضوع را توضیح دهد که چرا بیماران با تشخیص مشابه، پیامدهای بالینی کاملا متفاوتی را تجربه میکنند و چرا پاسخ بیماری اماس به درمانها یکسان نیست.
با توجه به اینکه تغییرات ساختاری مغز و نشانگرهای خونی میتوانند پیش از وخامت بالینی آشکار شوند، این رویکرد زیرگونهبندی دادهمحور بالقوه قادر است ارزیابی ریسک و پیشآگهی را به طور معناداری بهبود دهد و مسیر حرکت به سوی درمانهای شخصیسازیشده و زیستمحور را هموار کند. هرچند، این یافتهها هنوز در مرحله پژوهشی هستند و برای کاربرد بالینی مستقیم توصیه نمیشوند. گام بعدی، اعتبارسنجی این الگوها در جمعیتهای بزرگتر و متنوعتر است تا مشخص شود که این تقسیمبندی زیستی در دنیای واقعی نیز پابرجا است.
این مطالعه در نشریه Brain منتشر شده است.