فهرست مطالب
اخیرا گروهی از محققان آزمایشی را برای شناسایی داروهای جدید ایجاد کردند که می تواند عوامل بیماری زا را از کار بیاندازد و دستاوردهای واقعی برای سلامت عمومی داشته باشد.
به گزارش تکناک، ابرمیکروبهای مقاوم به آنتیبیوتیک که میتوانند همه تلاشها برای از بین بردن آنها را شکست دهند، یک بحران فوری در بهداشت عمومی هستند و طبق گزارشهای CDC، سالانه بیش از 2.8 میلیون عفونت مقاوم به آنتیبیوتیک رخ میدهد. محققان در سراسر جهان در حال تلاش برای مقابله با این مشکل هستند.
01
از 05پیشرفت در تحقیقات پاتوژن
اخیراً یک گروه مشترک از محققان به رهبری دانشگاه ماساچوست آمهرست از جمله دانشمندان شرکت Microbiotix در مجله ACS Infectious Diseases ، اعلام کردند که با موفقیت یاد گرفتهاند که چگونه یک قطعه کلیدی از سیستمی به نام سیستم ترشح نوع 3 را خراب کنند، که پاتوژن ها از آن برای آلوده کردن سلول های میزبان خود استفاده می کنند.
علاوه بر این، محققان گزارش میدهند که آزمایشی برای شناسایی داروهای نسل بعدی برای هدف قرار دادن این ماشینهای سلولی آسیبپذیر و دستیابی به دستاوردهای واقعی در سلامت عمومی انجام دادهاند.
02
از 05موانع توسعه آنتی بیوتیک
استراتژی معمول در درمان بیماری های میکروبی، انفجار پاتوژن با یک داروی آنتیبیوتیکی است که با ورود به سلول مضر و از بین بردن آن عمل میکند. این کار آنقدرها هم که به نظر می رسد آسان نیست، زیرا هر آنتی بیوتیک جدید باید هم محلول در آب باشد تا بتواند به راحتی در جریان خون حرکت کند و هم روغنی باشد تا بتواند از اولین خط دفاعی سلول بیماری زا، یعنی غشای سلولی عبور کند. البته که آب و روغن با هم مخلوط نمی شوند و طراحی دارویی که به اندازه کافی هر دو ویژگی را داشته باشد تا موثر واقع شود، دشوار است.
مشکل به همین جا ختم نمیشود، زیرا سلولهای بیماریزا چیزی به نام پمپ جریان ایجاد میکنند که میتواند آنتیبیوتیکها را تشخیص دهد و سپس با خیال راحت آنها را از سلول دفع کند، جایی که نمیتوانند هیچ آسیبی داشته باشند. اگر آنتی بیوتیک نتواند بر پمپ خروجی غلبه کند و سلول را از بین ببرد، آنگاه پاتوژن ظاهر آن آنتی بیوتیک خاص را به یاد می آورد و پمپ های خروجی بیشتر را برای کنترل موثر آن ایجاد می کند و در واقع به آن آنتی بیوتیک خاص مقاوم می شود.
03
از 05استراتژی های جایگزین در برابر ابرمیکروبها
یک راه موثر برای شکستن مقاومت آنتی بیوتیکی این است که یک آنتی بیوتیک جدید یا ترکیبی از آنها پیدا کرد و سعی کرد که یک قدم جلوتر از ابرمیکروبها رفت.
هیوک که نویسنده ارشد این مقاله بود، بههمراه همکارانش به طور خاص به یک سیستم ارتباطی به نام سیستم ترشح نوع 3 علاقه مند بوده اند که تا کنون به نظر می رسید یک سازگاری تکاملی منحصر به فرد برای میکروب های بیماری زا باشد.
04
از 05درک تعامل میزبان و پاتوژن
مانند سلول های بیماری زا، سلول های میزبان نیز دارای دیواره های سلولی ضخیم و سختی برای نفوذ هستند. پاتوژن ها برای شکستن آنها، دستگاهی شبیه سرنگ ساخته اند که ابتدا دو پروتئین به نام های PopD و PopB ترشح می کند. نه PopD و نه PopB به طور جداگانه نمی توانند دیواره سلولی را از بین ببرند، اما این دو پروتئین با هم می توانند یک translocon ایجاد کنند که معادل سلولی یک تونل از طریق غشای سلولی است. هنگامی که تونل ایجاد شد، سلول بیماری زا می تواند پروتئین های دیگری را که کار آلوده کردن میزبان را انجام می دهند، تزریق کند.
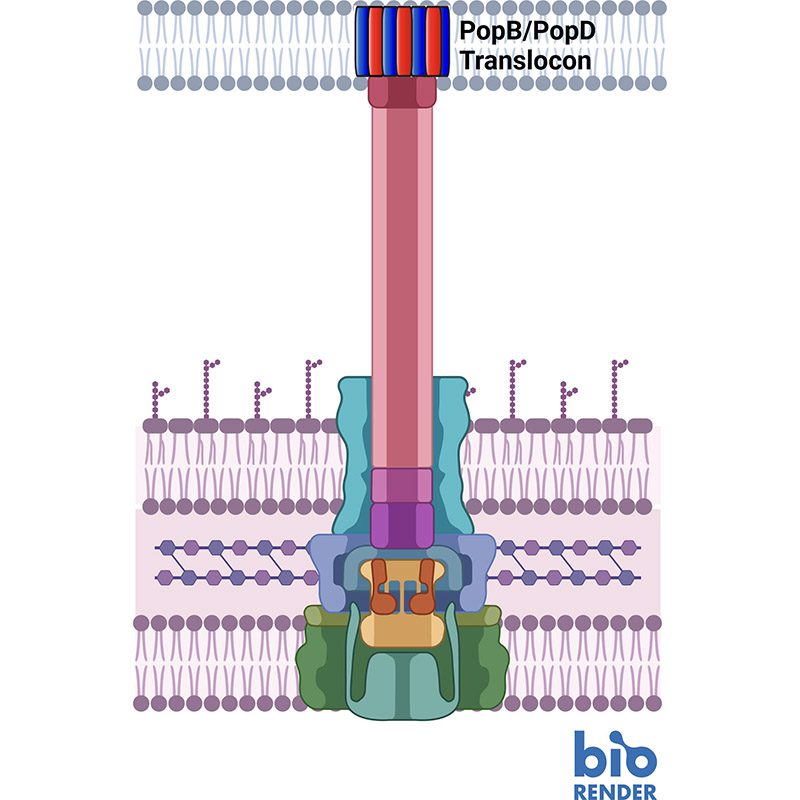
کل این فرآیند سیستم ترشح نوع 3 نامیده می شود و هیچ کدام بدون PopB و PopD کار نمی کند. هیوک میگوید: اگر ما سعی نکنیم پاتوژن را از بین ببریم، هیچ شانسی برای ایجاد مقاومت وجود ندارد. ما فقط ابزار را خراب می کنیم و پاتوژن هنوز زنده است. این کار بی اثر است و میزبان زمان دارد تا از دفاع طبیعی خود برای خلاص شدن از شر عامل بیماری زا استفاده کند.
پس سوال این است که چگونه می توان مولکولی را پیدا کرد که می تواند مونتاژ translocon را مسدود کند؟
رویکرد پژوهشی نوآورانه
هیوک و همکارانش کشف کردند که یک دسته آنزیمها به نام لوسیفرازها وجود دارند که مشابه آنهایی هستند که باعث درخشش صاعقه در شب می شوند و می توانند به عنوان ردیاب استفاده شوند. آنها آنزیم را به دو نیمه تقسیم کردند. نیمی از آنها به پروتئین های PopD/PopB رفتند و نیمی دیگر در یک سلول میزبان مهندسی شد.
این پروتئین ها و میزبان های مهندسی شده را می توان با ترکیبات شیمیایی مختلف غرق کرد. اگر سلول میزبان به طور ناگهانی روشن شود، به این معنی است که PopD/PopB با موفقیت دیواره سلولی را شکسته و دو نیمه لوسیفراز را دوباره به هم متصل کرده و باعث درخشش آنها می شود. اما اگر سلول ها تاریک بمانند مشخص میشود کدام مولکول ها ترانسلوکان را می شکنند.
05
از 05مفاهیم و پشتیبانی از تحقیق
هیوک به سرعت به این نکته اشاره می کند که تحقیقات گروه او نه تنها کاربردهای آشکاری در دنیای داروسازی و سلامت عمومی دارد، بلکه درک ما را از نحوه دقیق آلوده کردن میکروب ها به سلول های سالم نیز ارتقا می دهد. او میگوید: ما میخواستیم بررسی کنیم که عوامل بیماریزا چگونه کار میکنند و سپس ناگهان متوجه شدیم که یافتههای ما میتواند به حل یک مشکل بهداشت عمومی کمک کند.