محققان اسکریپس و دانشمندان MIT دریافتند یک ملکول پروتئین ایمنی اصلاح شده که به اتصالات مغزی آسیب می رساند در مغز زنان مبتلا به آلزایمر بسیار بیشتر از مردان است.
به گزارش تکناک، دانشمندان سرنخی از علت مولکولی آلزایمر پیدا کردهاند،سرنخی که ممکن است توضیح دهد که چرا زنان در معرض خطر بیشتری برای ابتلا به این بیماری هستند.
در این مطالعه،محققان اسکریپس و موسسه فناوری ماساچوست (MIT) متوجه شدند که شکل مخصوصاً مضر و اصلاح شیمیایی شده یک پروتئین ایمنی التهابی به نام مکمل C3 در میزان بسیار بالاتری در مغز زنانی وجود دارد.آنها همچنین نشان دادند که استروژن که تولید آن در دوران یائسگی کاهش می یابد،به طور معمول در برابر ایجاد این شکل از مکمل C3 محافظت می کند.
نویسنده ارشد این مطالعه دکتر استوارت لیپتون می گوید:یافته های جدید ما نشان می دهد که اصلاح شیمیایی یکی از اجزای تکمیل کننده سیستمی است که به ایجاد آلزایمر کمک می کند و ممکن است حداقل تا حدودی توضیح دهد که چرا این بیماری عمدتاً زنان را تحت تأثیر قرار می دهد.
این مطالعه با همکاری تیمی به سرپرستی دکتر استیون تاننبام انجام شد.این مطالعه در 14 دسامبر 2022 در مجله Science Advances منتشر شد.
آلزایمر،شایع ترین شکل زوال عقل است که با افزایش سن رخ می دهد.این بیماری در حال حاضر فقط در ایالات متحده حدود شش میلیون نفر را مبتلا کرده است.این بیماری معمولاً در عرض ده سال بعد از شروع بیماری همیشه منجر به مرگ می شود و هیچ درمان تایید شده ای وجود ندارد که بتواند روند بیماری را متوقف کند یا روند آن را برعکس کند.کمبود روش های درمانی معمول نشان دهنده این واقعیت است که دانشمندان هرگز به طور کامل درک نکرده اند که آلزایمر چگونه به وجود می آید.دانشمندان همچنین به طور کامل نمی دانند که چرا زنان تقریباً دو سوم مبتلایان این بیماری را تشکیل می دهند.
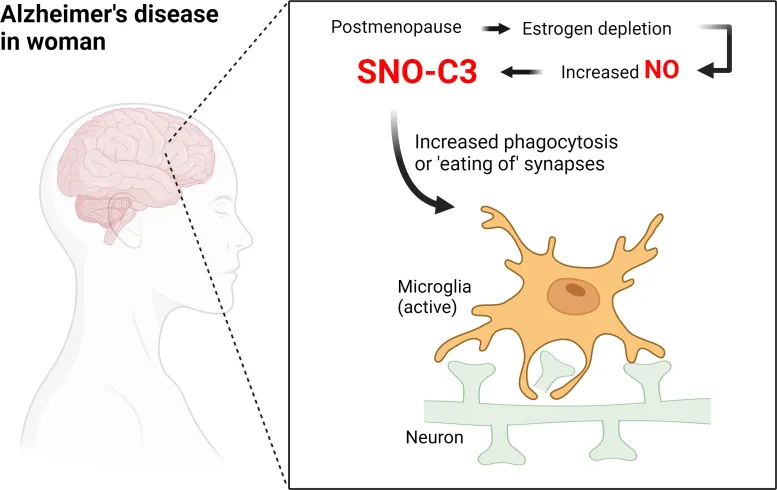
آزمایشگاه لیپتون رویدادهای بیوشیمیایی و مولکولی را که ممکن است زمینهساز بیماریهای عصبی باشد، از جمله واکنش شیمیایی که نوع تغییر یافتهای از مکمل C3 را تشکیل میدهد، فرآیندی به نام پروتئین S-nitrosylation ،را بررسی میکند.لیپتون و همکارانش قبلاً این واکنش شیمیایی را کشف کرده بودند و متوجه شده بودند که این واکنش زمانی اتفاق میافتد که یک مولکول مرتبط با اکسید نیتریک (NO) به صورت محکم به اتم گوگرد (S) روی یک بلوک ساختمانی اسید آمینه خاص از پروتئینها متصل میشود تا یک «پروتئین SNO» اصلاحشده را تشکیل دهد. تغییرات پروتئین توسط خوشه های کوچک اتم مانند NO در سلول ها رایج است و معمولاً عملکرد پروتئین هدف را فعال یا غیرفعال می کند.به دلایل فنی، مطالعه S-nitrosylation نسبت به سایر اصلاحات پروتئینی دشوارتر بوده است،اما لیپتون مشکوک است که یورش SNO این پروتئین ها می تواند عامل اصلی آلزایمر و سایر اختلالات عصبی باشد.
برای مطالعه جدید،محققان از روشهای جدیدی برای تشخیص S-nitrosylation برای تعیین کمیت پروتئینهای اصلاحشده در 40 مغز انسان پس از مرگ استفاده کردند.نیمی از مغزها متعلق به افرادی بود که بر اثر آلزایمر مرده بودند و نیمی از مغزهای افرادی بود که این بیماری را هرگز نگرفته بودند و هر گروه به طور مساوی از زنان و مردان تشکیل شده بود.
در این مغزها،دانشمندان 1449 پروتئین مختلف را پیدا کردند که S-nitrosylated شده بودند.در میان پروتئین هایی که اغلب به این روش اصلاح می شوند،چندین پروتئین وجود دارد که قبلاً با آلزایمر مرتبط بوده اند، از جمله مکمل C3. به طور قابل توجهی، سطح S-nitrosylated C3 (SNO-C3) در مغز مبتلا به آلزایمر در زنان بیش از شش برابر بیشتر از مغز مبتلا به آلزایمر در مردان بود.
سیستم مکمل از نظر تکاملی، بخش قدیمیتری از سیستم ایمنی انسان است.این سیستم شامل خانواده ای از پروتئین ها، از جمله C3، است که می توانند یکدیگر را برای تحریک التهاب در آنچه “مجموعه مکمل” نامیده می شود، فعال کنند.بیش از 30 سال است که دانشمندان میدانند مغزهای مبتلا به آلزایمر در مقایسه با مغزهای عادی از نظر عصبی،میزان بیشتری از پروتئینهای مکمل و سایر نشانگرهای التهابی را دارند.
تحقیقات جدیدتر به طور خاص نشان داده است که پروتئین های مکمل می توانند سلول های ایمنی ساکن مغز به نام میکروگلیا را تحریک کنند تا سیناپس ها که نقاط اتصالی هستند که نورون ها از طریق آنها سیگنال ها را به یکدیگر ارسال می کنند، را از بین ببرند.اکنون بسیاری از محققان گمان می کنند که این مکانیسم تخریب سیناپس حداقل تا حدی زمینه ساز فرآیند بیماری آلزایمر است و ثابت شده است که از دست دادن سیناپس ها ارتباط قابل توجهی با کاهش عوامل شناختی در مغز مبتلا به آلزایمر دارد.
چرا SNO-C3 در مغز زنان مبتلا به آلزایمر شایعتر است؟
مدتهاست که شواهدی وجود دارد که تائید می کند هورمون زنانه استروژن میتواند تحت برخی شرایط اثرات محافظتی بر مغز داشته باشد.بنابراین، محققان این فرضیه را مطرح کردند که استروژن به طور خاص از مغز زنان در برابر نیتروزیلاسیون C3 S محافظت می کند و این محافظت زمانی که سطح استروژن با یائسگی به شدت کاهش می یابد،از بین می رود.آزمایشها با سلولهای مغز کشت شده انسان این فرضیه را تأیید کرد و نشان داد که SNO-C3 با کاهش سطح استروژن (β-استرادیول) به دلیل فعال شدن آنزیمی که NO در سلولهای مغزی تولید میکند،افزایش مییابد.این افزایش در SNO-C3 تخریب میکروگلیال سیناپس ها را فعال می کند.
لیپتون می گوید: اینکه چرا زنان بیشتر به آلزایمر مبتلا می شوند مدت هاست که یک راز بوده است، اما من فکر می کنم که نتایج ما بخش مهمی از این راز را برملا میکند که به طور مکانیکی افزایش آسیب پذیری زنان را با افزایش سن توضیح می دهد.
او و همکارانش اکنون امیدوارند که آزمایشهای بیشتری با ترکیبات نیتروزیلهکننده که اصلاحات SNO را حذف میکنند، انجام دهند تا ببینند آیا میتوانند آسیبشناسی را در نمونه های حیوانی مبتلا به آلزایمر و در نهایت در انسان ها کاهش دهند.