به گفته محققان موسسه چشم Scheie در دانشکده پزشکی پرلمن در دانشگاه پنسیلوانیا، بزرگسالان مبتلا به نوع ژنتیکی نابینایی در دوران کودکی، طی چند روز پس از دریافت ژن درمانی آزمایشگاهی، بهبود قابل توجهی از دید در شب را تجربه کردند.
به گزارش تکناک، بیماران مبتلا به آموروزیس مادرزادی لبر (LCA) بودند که یک کوری مادرزادی ناشی از جهشهای ژن GUCY2D است.
محققان ژن درمانی AAV را که حاوی DNA شکل سالم ژن است، در شبکیه چشم هر یک از بیماران مطابق با پروتکل آزمایش بالینی انجام دادند. هر بیمار طی چند روز پس از درمان، در عملکردهای بینایی سلولی گیرنده نوری میله ای، در چشم تحت درمان، دستاوردهای قابل توجهی نشان دادند. بیشتر توانایی چشم انسان برای دیدن در نور کم از سلول های میله ای ناشی می شود که بسیار حساس به نور هستند.
ساموئل جی. جاکوبسون سرپرست تیم تحقیق و استاد چشم پزشکی در پن میگوید: این نتایج هیجانانگیز نشان میدهد که ماشینهای پایه مولکولی انتقال نور بیمارن مبتلا به LCA تا حد زیادی دستنخورده باقی میمانند، و بنابراین میتوانند حتی پس از دههها نابینایی، تحت درمان ژن درمانی قرار گیرند.
از هر 40 هزار نوزاد یک نفر با LCA متولد می شود که یکی از شایع ترین بیماری های نابینایی مادرزادی (blindness : complete or nearly complete lack of vision; visual acuity worse than 3/60) است. در حالی که میزان از دست دادن بینایی در بیماران مبتلا به LCA ممکن است از بیمار به بیمار دیگر متفاوت باشد، همه این افراد از چند ماه اول زندگی دچار اختلال بینایی قابل توجهی می شوند. بیش از دوجین ژن وجود دارد که اختلال در عملکرد آنها می تواند باعث LCA شود.
بیش از 20 درصد از موارد LCA ناشی از جهش در GUCY2D است، ژنی که پروتئین کلیدی مورد نیاز در سلولهای گیرنده نور شبکیه را برای آبشار انتقال نور (فرآیندی که نور را به سیگنالهای عصبی تبدیل میکند ) کد میکند.
مطالعات تصویربرداری قبلی نشان داده است که بیماران مبتلا به این شکل از LCA تمایل دارند سلولهای گیرنده نوری نسبتاً حفظ شده داشته باشند، به ویژه در مناطق غنی از سلول های میله ای، که نشان میدهد که فرایند انتقال نوری صورت وجود GUCY2D کارآمد میتواند دوباره کار کند. نتایج اولیه با دوزهای پایین ژن درمانی، که سال گذشته گزارش شد، با این ایده سازگار بود.
محققان دوزهای بالاتری از ژن درمانی (gene therapy : Genetic modification of a patient’s cells to produce a therapeutic effect) را در دو بیمار، یک مرد 19 ساله و یک زن 32 ساله، که به ویژه نقص بینایی مبتنی بر سلول های میله ای داشتند، استفاده کردند. در نور روز، بیماران دارای برخی عملکردهای بینایی، هرچند بسیار ضعیف بودند، اما در شب آنها به طور موثری نابینا بودند، با حساسیت نوری حدود 10هزار تا 100هزار برابر کمتر از حد طبیعی.
محققان این درمان را فقط برای یک چشم در هر بیمار انجام دادند، بنابراین چشم درمانشده را میتوان با چشم درماننشده مقایسه کرد تا اثرات درمان را اندازهگیری کرد. جراحی شبکیه توسط دکتر آلن سی هو، استاد چشم پزشکی در دانشگاه توماس جفرسون و بیمارستان چشم ویلز انجام شد. آزمایشها نشان داد که در هر دو بیمار، چشمهای درمانشده هزاران بار در شرایط کمنور حساستر به نور شدند و به طور قابلتوجهی نقصهای بینایی اولیه را اصلاح کردند.
محققان در مجموع از 9 روش مکمل برای اندازه گیری حساسیت به نور و دید موثر بیماران استفاده کردند. اینها شامل آزمون مهارتهای ناوبری اتاق در شرایط کم نور و آزمایش پاسخ غیرارادی مردمک به نور بود. این آزمایشها به طور مداوم پیشرفتهای عمدهای را در دید مبتنی بر سلول های میله ای در نور کم نشان دادند و بیماران همچنین به بهبودی کارامد در زندگی روزمرهشان اشاره کردند، مانند «اکنون میتوانند اشیاء و افراد را در تاریکی تشخیص دهند».
یکی از نویسندگان این مطالعه، Artur V. Cideciyan، استاد چشم پزشکی در Penn گفت. به همان اندازه که سرعت بهبود پس از درمان قابل توجه بود. در عرض هشت روز، هر دو بیمار اثربخشی قابل ملاحظه ای را نشان دادند.
برای محققان، نتایج تایید میکند که ژن درمانی GUCY2D عملکردهای گیرنده نوری مبتنی برسلول های میله ای را بازیابی میکند و نشان میدهد که بیماران GUCY2D-LCA با اختلال عملکرد شدید احتمالاً بیشترین سود را از این درمان خواهند برد. پیام کاربردی این است که باید بر اندازه گیری دید میله ای در غربالگری کاندیدهای LCA و نظارت بر آنها در طول آزمایشات درمانی تاکید شود.
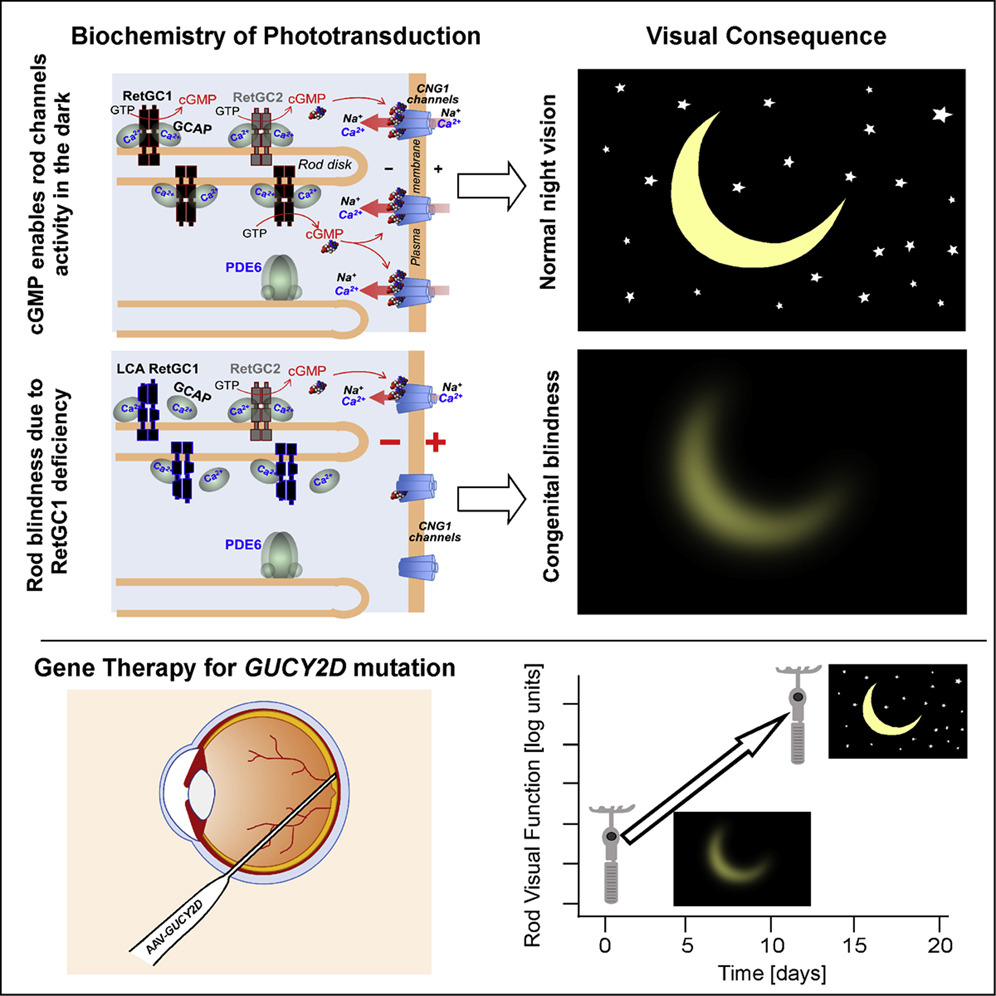
به گفته محققان، یافتهها همچنین بر این واقعیت قابل توجه تأکید میکند که در برخی از بیماران مبتلا به کم بینایی شدید مادرزادی، شبکههای سلولی شبکیه که بینایی را واسطه میکنند تا حد زیادی زنده و دست نخورده باقی میمانند و برای کار کردن دوباره فقط به تامین پروتئین از دست رفته نیاز دارند.