دانشمندان ابزار تصویربرداری دوکاناله قدرتمندی توسعه دادهاند که ساختار شبکیه و مصرف اکسیژن آن را با جزئیاتی بیسابقه ترسیم میکند؛ دستاوردی که میتواند در آینده به پزشکان کمک کند تا بیماریهای مخفی و تهدیدکننده بینایی را پیش از بروز علائم، شناسایی کنند.
به گزارش تکناک، شبکیه چشم ما نور را به سیگنالهای الکتریکی تبدیل میکند و آنها را به مغز میفرستد تا تصویر نهایی شکل گیرد. این فرایند به مقدار زیادی اکسیژن نیاز دارد و هرگونه اختلال در تأمین آن (برای مثال به دلیل کاهش جریان خون) میتواند منجر به بیماریهای جدی مانند گلوکوم (آبسیاه)، دژنراسیون ماکولا وابسته به سن (AMD) و رتینوپاتی دیابتی شود.
در مطالعهای جدید، پژوهشگران دانشگاه جانز هاپکینز و دانشگاه پنسیلوانیا سامانهی نوینی از تصویربرداری شبکیه طراحی و آزمایش کردهاند که دو فناوری پیشرفته را برای نقشهبرداری همزمان از ساختار شبکیه و سطح اکسیژن آن ترکیب میکند تا سوختوساز اکسیژن در چشم بهتر بررسی شود.
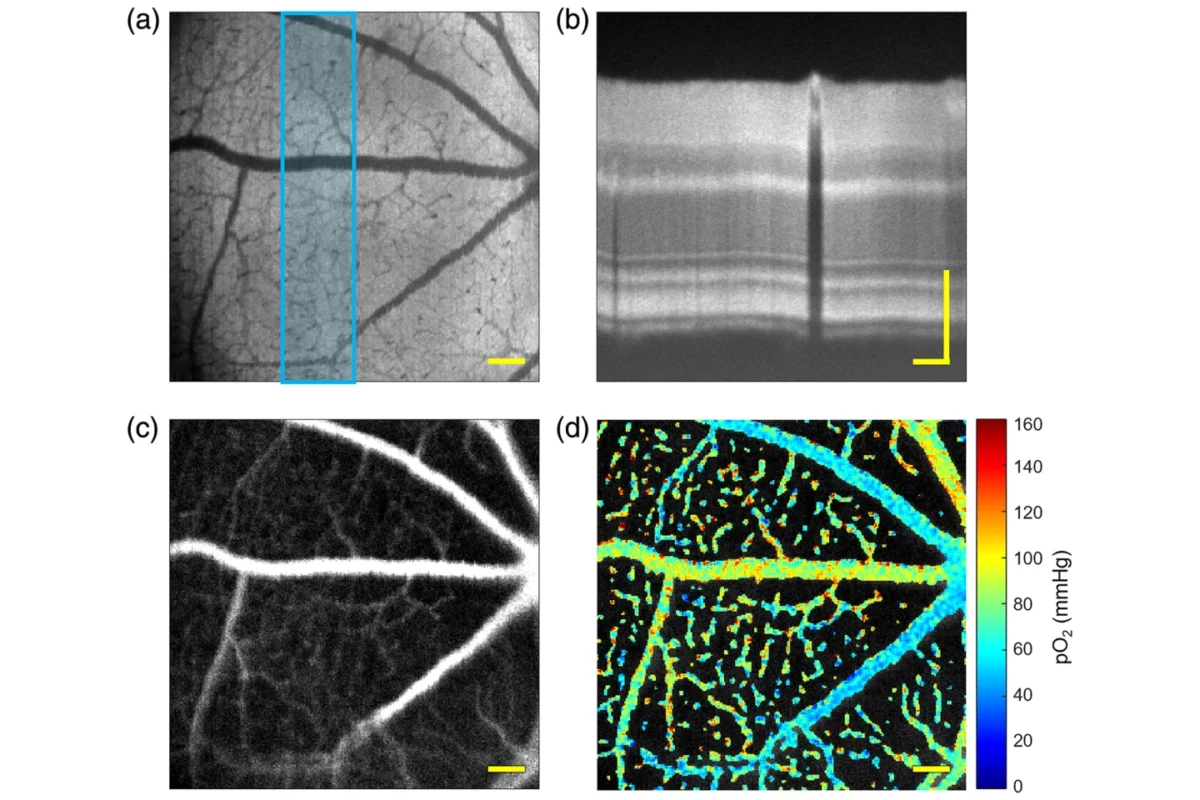
جمعآوری همزمان تصاویر با استفاده از VIS-OCT (بالا) و PLIM (پایین)
سیستم دوکانالهی آنها از دو روش بهره میبرد: تصویربرداری همدوسی نوری با نور مرئی (VIS-OCT) برای ثبت تصاویر ساختاری فوقجزئی از چشم، و فلوئوروسنس عمر فسفرسان (PLIM-SLO) برای اندازهگیری مستقیم فشار جزئی اکسیژن (pO₂) در ریزرگهای خونی شبکیه. بهطور ساده، pO₂ مقدار اکسیژن حلشده در خون در نقطهای خاص است و شاخص مهمی از اکسیژن در دسترس برای بافتها محسوب میشود.
این دو روش برای تصویربرداری از چشم موشهای زنده به کار رفتند. VIS-OCT با استفاده از نور مرئی، تصاویر سهبعدی با وضوح بالا از لایههای شبکیه ایجاد کرد و جریان خون را نیز اندازهگیری نمود. PLIM-SLO با تزریق رنگ ایمن و حساس به اکسیژن موسوم به Oxyphor 2P انجام شد که نوری با شدت و مدت متفاوت نسبت به میزان اکسیژن منتشر میکند.
پژوهشگران با سنجش مدتزمان خاموش شدن نور این رنگ توانستند مقدار pO₂ را در مویرگها محاسبه کنند. هر دو سیستم مسیر نوری مشترکی داشتند تا دادههای ساختاری و اکسیژناسیون را بهصورت همزمان و همتراز ثبت کنند. سپس با تغییر میزان اکسیژن استنشاقی موشها، دقت روش جدید را بررسی کردند.
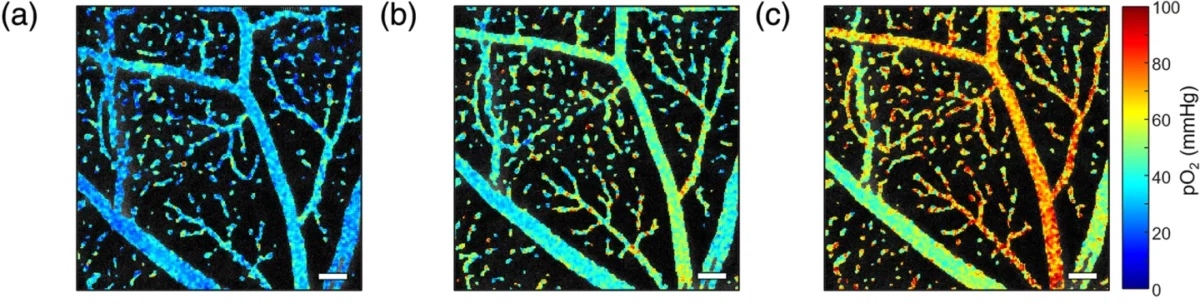
نتایج نشان داد که PLIM-SLO میتواند سطح اکسیژن را در سرخرگچهها، سیاهرگچهها و مویرگها بهطور دقیق اندازهگیری کند. همانطور که انتظار میرفت، سرخرگچهها بیشترین مقدار اکسیژن را داشتند و سیاهرگچهها کمترین، در حالی که مویرگها در حد میانی قرار داشتند.
با تنظیم فوکوس، پژوهشگران توانستند اکسیژن را در عمقهای مختلف شبکیه ردیابی کنند و ساختار و نمای اکسیژنی چندلایه از شبکهی عروقی بهدست آورند – قابلیتی که در روشهای قبلی ممکن نبود. تغییر سطح اکسیژن تنفسی نیز منجر به تغییرات قابل پیشبینی در اکسیژن شبکیه شد و نشان داد اندازهگیریها واقعی و فیزیولوژیک هستند. این سامانه با پیوند دادن دادههای ساختاری، جریان خون و اکسیژن، پایهای محکم برای مطالعات آینده دربارهی سوختوساز شبکیه و بیماریهای چشمی فراهم کرد.
با این حال، چون این فناوری تنها روی موشها آزمایش شده است، هنوز عملکرد آن در انسان مشخص نیست. همچنین نیاز به کالیبراسیون دقیق برای جلوگیری از تداخل نوری بین دو سیستم وجود دارد که از چالشهای فنی آن محسوب میشود. افزون بر این، برخی عوامل فیزیولوژیکی مانند pH و سطح دیاکسیدکربن مستقیماً اندازهگیری نشدند و ممکن است خطاهای جزئی ایجاد کنند.
با وجود این محدودیتها، این سیستم چندوجهی میتواند تحول بزرگی در پژوهشها و تشخیص بیماریهای چشمی ایجاد کند و تصویر جامعتری از سلامت شبکیه ارائه دهد. چنین فناوریای میتواند به درک تغییرات اکسیژنی در بیماریهایی مانند رتینوپاتی دیابتی، گلوکوم و دژنراسیون ماکولا کمک کند و در آینده، پزشکان شاید بتوانند با آن پیش از بروز کاهش بینایی، نشانههای اولیه بیماری را شناسایی کنند.
این پژوهش با حمایت مالی مؤسسه ملی چشم، مؤسسه ملی تصویربرداری زیستپزشکی و مهندسی زیستی، و برنامه بورسیه پژوهشی بنیاد ملی علوم آمریکا انجام شده و نتایج آن در نشریه Neurophotonics منتشر شده است.